واکنشی را که در آن ، تبادل الکترون صورت میگیرد، واکنش اکسیداسیون- احیا Oxidation - reduction نامیده میشود.

تبادل الکترونی
پس در نتیجه تبادل الکترونی بین یک اکسید کننده و یک احیا کننده یک واکنش شیمیایی رخ می دهد.
فرآیند اکسیداسیون (اکسایش)
فرآیندی است که در آن یک جسم (اکسید کننده) الکترون میگیرد و عدد اکسایش یک اتم افزایش مییابد.
فرآیند احیا (کاهش)
فرایندی است که در آن یک جسم (احیا کننده) الکترون از دست میدهد و عدد اکسایش یک اتم کاهش مییابد.
مثالی از واکنشهای اکسایش و کاهش
بر این اساس ، واکنش زیر یک واکنش اکسایش و کاهش میباشد. چون عدد اکسایش اتم S از صفر به +4 افزایش پیدا میکند و میگوییم گوگرد اکسید شده است و عدد اکسایش اتم O از صفر به -2 کاهش پیدا کرده است و میگوییم اکسیژن کاهیده شده است:
که در آن ، در طرف اول عدد اکسیداسیون هر دو ماده صفر و در طرف دوم ، عدد اکسیداسیون گوگرد در ترکیب +4 و اکسیژن ، -2 است.
اما در واکنش زیر اکسایش- کاهش انجام نمیشود، زیرا تغییری در عدد اکسایش هیچ یک از اتمها به وجود نیامده است:
که در SO2 ، عدد اکسیداسیون S و O بترتیب ، +4 و -2 و در آب ، عدد اکسیداسیون H و O بترتیب +1 و -2 و در اسید در طرف دوم ، عدد اکسیداسیون H و S و O بترتیب ، +1 ، +4 و -2 است.
عامل اکسنده و عامل کاهنده
با توجه به چگونگی نسبت دادن اعداد اکسایش ، واضح است که نه عمل اکسایش و نه عمل کاهش بتنهایی انجام پذیر نیستند. چون یک ماده نمیتواند کاهیده شود مگر آن که همزمان ماده ای دیگر ، اکسید گردد، ماده کاهیده شده ، سبب اکسایش است و لذا عامل اکسنده نامیده میشود و مادهای که خود اکسید میشود، عامل کاهنده مینامیم.
بعلاوه در هر واکنش ، مجموع افزایش اعداد اکسایش برخی عناصر ، باید برابر مجموع کاهش عدد اکسایش عناصر دیگر باشد. مثلا در واکنش گوگرد و اکسیژن ، افزایش عدد اکسایش گوگرد ، 4 است. تقلیل عدد اکسایش ، 2 است، چون دو اتم در معادله شرکت دارد، کاهش کل ، 4 است.
موازنه معادلات اکسایش- کاهش
دو روش برای موازنه واکنشهای اکسایش- کاهش بکار برده میشود: روش یون- الکترون و روش عدد اکسایش.
روش یون- الکترون برای موازنه معادلات اکسایش- کاهش
در موازنه معادلات به روش یون- الکترون ، دو دستور کار که کمی با هم متفاوتاند، مورد استفاده قرار میگیرد. یکی برای واکنشهایی که در محلول اسیدی انجام میگیرد و دیگری برای واکنشهایی که در محلول قلیایی صورت میپذیرد.
- مثالی برای واکنشهایی که در محلول اسیدی رخ میدهد، عبارت است:
این واکنش موازنه نشده ، طی عملیات زیر موازنه می شود:
_ابتدا معادله را به صورت دو معادله جزئی که یکی برای نشان دادن اکسایش و دیگری برای نشان دادن کاهش است، تقسیم کرده و عنصر مرکزی را در هر یک از این نیم واکنش ها موازنه می کنیم:
_اتمهای O و H را موازنه میکنیم. در سمتی که کمبود اکسیژن دارد، به ازای هر اکسیژن یک H2O اضافه میکنیم و در سمتی که کمبود هیدروژن دیده میشود، با افزودن تعداد مناسب +H آن را جبران می کنیم. در مثال بالا، طرف راست ، معادله جزئی اول 7 اتم اکسیژن کم دارد، پس به طرف مزبور 7H2O افزوده میشود. پس اتمهای H معادله جزئی اول را با اضافه کردن چهارده +H به طرف چپ معادله، موازنه میکنیم. معادله جزئی دوم ، بصورت نوشته شده ، از لحاظ جرمی ، موازنه است:
_در مرحله بعد ، باید معادلات جزئی را از نظر بار الکتریکی موازنه میکنیم. در معادله جزئی جمع جبری بار الکتریکی طرف چپ برابر +12 و در طرف راست +6 است. 6 الکترون به سمت چپ اضافه میشود تا موازنه بار برای معادله جزئی اول حاصل شود. معادله دوم با افزودن دو الکترون به طرف راست ان موازنه میشود، ولی چون تعداد الکترونهای از دسترفته در یک معادله جزئی باید برابر تعداد الکترونهای بدست آمده در معادله جزئی دیگر باشد، بنابراین طرفین معادله جزئی دوم را در 3 ضرب میکنیم:
_معادله نهایی ، با افزایش دو معادله جزئی و حذف الکترونها بدست میآید:
- مثالی برای واکنش هایی که در محلول قلیایی صورت میگیرد:
_معادله به دو معادله جزئی تقسیم می شود:
_برای موازنه H و O در این واکنشها ، درسمتی که کمبود اکسیژن دارد، به ازای هر اتم اکسیژن -2OH و سمت دیگر یک H2O اضافه میکنیم و در سمتی که کمبود هیدروژن دارد به ازای هر اتم هیدروژن ، یک H2O و در سمت مقابل یک -OH اضافه میکنیم. سمت راست معادله جزئی اول دو اتم O کم دارد. لذا -4OH به سمت راست و 2H2Oبه سمت چپ میافزاییم:
برای موازنه جرمی معادله جزئی دوم ، باید چهار اتم هیدروژن به سمت راست اضافه کنیم، لذا 4H2O به سمت راست و -4OH به سمت چپ اضافه میکنیم:
_برای موازنه بار الکتریکی ، هر جا لازم است، الکترون اضافه میکنیم و در این جا بطرف چپ معادله جزئی اول ، سه الکترون و بطرف چپ معادله جزئی دوم ، چهار الکترون افزوده میشود و برای موازنه کردن الکترونهای بدست آمده و از دست رفته ، مضرب مشترک گرفته و معادله اول را در 4 و معادله دوم را در 3 ، ضرب میکنیم:
_جمع دو معادله جزئی، معادله نهایی را بدست میدهد:
روش عدد اکسایش برای موازنه واکنشهای اکسایش- کاهش
موازنه شامل سه مرحله است. برای مثال واکنش نیتریک اسید و هیدروژن سولفید را در نظر میگیریم. معادله موازنه نشده به قرار زیر است:
_برای تشخیص اتمهایی که کاهیده یا اکسیده میشوند، اعداد اکسایش آنها را از معادله بدست میآوریم:
نیتروژن کاهیده شده (از +5 به +2 ، کاهشی معادل 3 در عدد اکسایش) و گوگرد اکسید شده است (از -2 به صفر ، یعنی افززایشی معادل 2 در عدد اکسایش).
_برای ان که مجموع کاهش در اعداد اکسایش برابر با مجموع افزایش این اعداد باشد، ضرایبی متناسب به هر ترکیب نسبت میدهیم:
_موازنه معادله را ، با بررسی دقیقتر ، کامل میکنیم. در مراحل پیشین تنها موازنه موادی مطرح شد که اعداد اکسایش انها تغییر میکند. در این مثال ، هنوز ضریبی برای H2O در نظر گرفته نشده است. ولی ملاحظه میشود که در سمت چپ واکنش 8 اتم H وجود دارد. همان سمت 4 اتم O نیز اضافی دارد. بنابراین ، برای تکمیل موازنه ، باید در سمت راست معادله ، 4H2O نشان داده شود:
پس معادلات اکسایش- کاهش مانند واکنشهای الکتروشیمیایی و واکنش های یونی را میتوان با یکی از دو روش نامبرده موازنه کرد.
نگاه اجمالی
بشر از دیر باز با مفهوم ساده اسید آشنایی داشته است. در حقیقت این مواد، حتی قبل از آنکه شیمی به صورت یک علم در آید، شناخته شده بودند. اسیدهای آلی همچون سرکه و آبلیمو و آب غوره از قدیم معروف بودند. اسیدهای معمولی مانند اسید سولفوریک ، اسید کلریدریک و اسید نیتریک بوسیله کیمیاگران قدیم ساخته شدند و بصورت محلول در آب بکار رفتند. برای مثال اسید سولفوریک را جابربن حیان برای نخستین بار از تقطیر بلورهای زاج سبز (FeSO4.7H2O) و حل کردن بخارات حاصل در آب ، بدست آورد.
در طی سالیان متمادی بر اساس تجربیات عملی لاووازیه (A.L.Lavoisier) چنین تلقی میگردید که اجزاء ساختمان عمومی کلیه اسیدها از عنصر اکسیژن تشکیل گردیده است. اما بتدریج این موضوع از نظر علمی روشن و اعلام گردید که چنانچه این موضوع صحت داشته باشد، بر خلاف عقیده اعلام شده در مورد اکسیژن ، این عنصر هیدروژن است. در حقیقت ، تعریف یک اسید بنا به فرمول اعلام شده از سوی لیبیگ (J. Von Liebig) در سال 1840 عبارت است از:
| موادی حاوی هیدروژن که میتوانند با فلزات واکنش نموده و گاز هیدروژن تولید نمایند. |
نظریه فوق مدت پنجاه سال مورد استناد بوده است. بعدها با پیشرفت علم شیمی ، مفاهیم جدیدی درباره اسیدها اعلام شده که در زیر به بررسی آنها خواهیم پرداخت.
خواص عمومی اسیدها
- محلول آبی آنها یونهای پروتون آزاد میکند.
- موادی هستند که از نظر مزه ترشند.
- کاغذ تورنسل را سرخ رنگ میکنند.
- با برخی فلزات مانند آهن و روی ترکیب شده گاز هیدروژن میدهند.
- با قلیاها (بازها) واکنش نموده و املاح را تشکیل میدهند.
- با کربنات کلسیم (مثلا به صورت سنگ مرمر) بشدت واکنش دارند، بطوریکه کف میکنند و گاز کربنیک آزاد مینمایند.
نظریه آرنیوس درباره اسیدها
زمانیکه مفاهیم یونیزاسیون ترکیبات شیمیایی در محلولهای آبی روشن گردید، مفهوم اسید بطور قابل ملاحظهای تغییر پیدا کرد. مطابق تعریف آرنیوس ، اسید ماده ایست که در آب یونیزه میشود و یون +H3O که گاهی بصورت +H نیز نشان داده میشود، تولید میکند.
آرنیوس قدرت اسیدی را نیز بر همین اساس تفسیر کرد و گفت که اسید قوی ، در محلولهای آبی تقریبا، بطور کامل یونیزه میشود. در صورتیکه که میزان تفکیک اسید ضعیف کمتر است. توجه کنید که مفهوم آرنیوس بر یونهای آب استوار است. بر اساس تعریف آرنیوس میتوان نقش اکسیدهای اسیدی را نیز تفسیر کرد.
اکسیدهای اسیدی
اکسیدهای بسیاری از غیرفلزات با آب واکنش داده و اسید تولید میکنند، در نتیجه این مواد را اکسیدهای اسیدی یا ایندرید اسید مینامند.
مفهوم آرنیوس ، به علت تاکید آن بر آب و واکنشهای محلولهای آبی ، با محدودیت روبهروست.
نظریه برونشتد- لوری درباره اسیدها
در سال 1923، یوهان برونشتد و تامس لوری ، مستقل از یکدیگر مفهومی گستردهتر برای اسیدها و بازها بیان کردند. بر اساس تعریف ، برونشتد - لوری ، اسید ماده ای است که یک پروتون به باز میدهد. اسیدها ممکن است مولکول یا یون باشند. با حذف پروتون ، اسید به باز (باز مزودج اسید 1) تبدیل میشود و با گرفتن پروتون ، باز اولیه ، یعنی باز 2 به اسید2 (اسید مزدوج باز 2) تبدیل میشود.
قدرت اسیدها ، بر میل آنها برای از دست دادن یا گرفتن پروتون استوار است. هر چه اسید قویتر باشد، باز مزدوج آن ضعیفتر است. در یک واکنش ، تعادل در جهت تشکیل اسید ضعیفتر است. اسید پرکلریک ، HClO4 ، قویترین اسید است، و باز مزدوج آن ، یعنی یون پرکلرات ، -ClO4 ، ضعیفترین باز میباشد و H2 ، ضعیفترین اسید و باز مزدوج آن یعنی یون هیدرید ، +H قویترین باز میباشد.
نظریه لوییس درباره اسیدها
گیلبرت لوییس مفهوم گستردهتری برای اسیدها در سال 1938 پیشنهاد داد که پدیده اسید - باز را از پروتون رها ساخت. طبق تعریف لوییس ، اسید مادهای است که بتواند با پذیرش یک زوج الکترون از باز ، یک پیوند کوولانسی تشکیل دهد. در نظریه لوییس به مفهوم زوج الکترون و تشکیل پیوند کووالانسی تاکید میشود. تعریف لوییس در مورد اسیدها بسیار گستردهتر از آن است که برونشتد عنوان نموده است. ترکیبات شیمیایی که میتوانند نقش اسید لوییس داشته باشند، عبارتند از:
قدرت اسیدی و ساختار مولکولی
به منظور بررسی رابطه بین ساختار مولکولی و قدرت اسیدی ، اسیدها را به دو نوع تقسیم میکنیم: هیدریدهای کووالانسی و اکسی اسیدها.
هیدریدها
برخی از ترکیبات کووالانسی دوتایی هیدروژندار (مانند HCl , H2) اسیدی هستند. دو عامل بر قدرت اسیدی هیدریدیک عنصر موثر است: الکترونگاتیوی عنصر و اندازه اتمی عنصر. قدرت اسیدی هیدریدهای عناصر یک تناوب ، از چپ به راست و همسو با الکترونگاتیوی عناصر ، افزایش مییابد. یک عنصر الکترونگاتیو ، الکترونهای بیشتری از هیدروژن میگیرد و خروج آن به صورت یک پروتون را سرعت میبخشد.
قدرت اسیدی هیدریدهای عناصر یک گروه، با افزایش اندازه اتم مرکزی افزایش مییابد. در تناوب دوم: NH3>H2O>HF در گروه VI به اینصورت است:
اکسی اسیدها
در این ترکیبات ، هیدروژن اسیدی به یک اتم O متصل است و تغییر در اندازه این اتم بسیار ناچیز است. بنابراین عامل کلیدی در قدرت اسیدی این اکسیاسیدها، به الکترونگاتیوی اتم Z مربوط میشود: H-O-Z .
اگر Z یک اتم غیرفلز با الکترونگاتیوی بالا باشد، سهمی در کاهش چگالی الکترونی پیرامون اتم O (علی رغم الکترونگاتیوی شدید اکسیژن) را دارد. این پدیده باعث میشود که اتم اکسیژن، با کشیدن چگالی الکترونی پیوند H-O از اتم H ، تفکیک آن را سرعت ببخشد و ترکیب را اسیدی بکند. هیپوکلرواسید ، HOCl ، اسیدی از این نوع است.
هرچه الکترونگاتیوی Z بیشتر باشد، الکترونهای پیوند H-O به میزان بیشتری از اتم H دور میشوند و حذف پروتون آسانتر است: HOCl > HOBr > HOI . در اکسی اسیدهایی که اتمهای اکسیژن بیشتری به Z متصل باشند، قدرت اسیدی با افزایش n ، زیاد میشود.
مهمترین اسیدهای قوی
مولکولهای این اسیدها و در محلولهای آبی رقیق کاملا یونیزه است. اسیدهای قوی متعارف عبارتند از: اسید کلریدریک ، یدیدریک ، نیتریک ، سولفوریک ، پرکلریک است.
مهمترین اسیدهای ضعیف
یونیزاسیون این اسیدها در آب کامل نمیباشد و هرگز به 100% نمیرسد. مثال متعارف آنها ، اسید استیک ، اسید کربنیک ، اسیدفلوریدریک ، اسید نیترو و تا حدودی اسید فسفریک است.
برخی از کاربردهای اسیدها
اسید سولفوریک
یکی از اسیدهای معدنی قوی با فرمول H2SO4 ، مایعی روغنیشکل و بیرنگ است. یک متاع سودمند صنعتی است که از آن در حد وسیعی در پالایش نفت و در کارخانجات تولید کننده کودها ، رنگها ، رنگدانهها ، رنگینهها و مواد منفجره استفاده میشود.
اسید استیک
یک اسید آلی بصورت مایعی تند و بی رنگ با فرمول CH3COOH ، که اساس ترشی سرکه نیز میباشد. قسمت اعظم اسیداستیک تولیدی دنیا ، مصرف واکنش با الکلها به منظور تولید استرهایی میگردد که از آنها بعنوان بهترین حلالها در رنگ و جلا استفاده میشود. همچنین در کارخانجات داروسازی، عمل آوردن لاستیک طبیعی و تهیه چرم مصنوعی و به عنوان حلال برای بسیاری از ترکیبات آلی از اسید استیک استفاده میشود.
اسید نیتریک
یک اسید قوی معدنی با فرمول HNO3 میباشد که این اسید در کارخانجات تولید کودهای نیترات و فسفات آمونیوم ، مواد منفجره نیترو ، پلاستیکها ، رنگینهها و لاکها کاربر دارد.
اسید سولفونیک
این اسیدها با فرمول عمومی HSO3R که R میتواند متان یا بنزن و ... باشد، محلول در آب ، غیر فرار و جاذب الرطوبهاند و به عنوان عوامل امولسیون کننده ، مواد افزودنی و روغنهای روان کننده و به عنوان جلوگیری از خوردگی و زنگ زدگی استفاده میگردد.
اسید کلریدریک
یکی از اسیدهای معدنی قوی با فرمول HCl ، که مایعی بیرنگ یا اندکی زردرنگ ، بسیار خورنده و غیر آتشگیر است. این اسید در آب ، الکل ، بنزن حل میشود و در اسیدی کردن (فعال کردن) چاههای نفت ، پاک کردن رسوبات دیگهای بخار ، صنایع غذایی ، تمیز کردن فلزات و ... استفاده میشود.
تئوری آزمایش
در روش تیتر کردن سلولی با غلظت مشخصی به محلول دیگر اضافه میشود تا واکنش شیمیایی بین دو ماده حل شده کامل گردد. محلولی که غلظت آن مشخص باشد، محلول استاندارد است. در عمل تیتر کردن ، محلول استاندارد را از یک بورت به محلولی که باید غلظت آن اندازه گرفته شود، میافزایند و این عمل تا وقتی ادامه دارد که واکنش بین محلول استاندار تیتر شونده کامل شود. پس با استفاده از حجم و غلظت محلول استاندارد و حجم محلول تیتر شونده ، غلظت محلول تیتر شونده را حساب میکنند.
وسایل لازم
- بورت 50 میلی لیتر
- بالون ژوژه 100 میلی لیتری و 50 میلی لیتری
- ارلن مایر 250 میلی لیتری
- بشر 100 میلی لیتری
- ترازوی دقیق
مواد شیمیایی لازم
- تیتر ازول کلریدریک اسید 0،1 نرمال
- سود
- اگزالیک اسید خالص
- فنل فتالئین
روش آزمایش
بخش اول : تعیین نرمالیته سود مجهول
نمونه مجهول سود (NaOH) در بالون ژوژه 100 میلی لیتری را با آب مقطر به حجم رسانده ، هم میزنیم. پس یک بورت 25 میلی لیتری را ابتدا با آب مقطر سپس با محلول سود تهیه شده شستشو میدهیم و توسط گیره به پایه متصل میکنیم. داخل بورت ، محلول سود ریخته ف محلول را در صفر تنظیم میکنیم.
- در نوک بورت نباید حباب هوا وجود داشته باشد. در صورت وجود داشتن هوا در نوک بورت باید شیر بورت را کمی باز کرد تا نوک بورت از مایع پر شود.
- در موقع خواندن بورت ، چشم باید در امتداد سطح مایع بوده و عدد مقابل خط زیر سطح مقعر مایع خوانده شود.
حال یک ارلن مایر که پیپت 10 میلی لیتری و با کلریدریک اسید 0،1 نرمال شستشو داده ایم، 10 میلی لیتر کلریدریک اسید 0،1 نرمال می ریزیم. سپس 2 قطره فنل فتالئین اضافه میکنیم. ارلن را زیر بورت قرار داده ، با دست چپ بشر بورت را باز میکنیم تا قطره قطره محلول سود به محلول اسید اضافه شود و با دست راست ، ارلن را بهآهستگی حرکت دورانی میدهیم. طی این عمل ، محلول داخل ارلن ، رنگ ارغوانی (صورتی رنگ) میشود و این نشانگر بازی شدن محلول داخل ارلن است. افزایش سود را متوقف کرده و حجم سود مصرفی را از روی بورت میخوانیم.
از فرمول زیر نرمالیته سود مجهول بهراحتی محاسبه میشود:
بخش دوم : تعیین نرمالیته اگزالیک اسید
یک گرم اگزالیک اسید را داخل بشر 100 میلی لیتری ریخته و کمی آب مقطر به آن اضافه میکنیم تا حل شود و سپس محلول را به یک بالون ژوژه 50 میلی لیتری انتقال داده و به حجم میرسانیم. توسط پیپت ژوژه ، 10 میلی لیتر از این محلول را داخل ارلن مایر 250 میلی لیتری میریزیم و دو قطره فنل فتالئین به آن اضافه میکنیم. سپس بورت را از سود با نرمالیته معلوم پر میکنیم و محلول داخل ارلن را با آن تیتر میکنیم.
روش تیتر کردن به این صورت است که طبق بخش اول ، سود را قطره قطره به محلول داخل ارلن افزوده تا صورتی کمرنگ ایجاد شود. سپس حجم بورت را یادداشت میکنیم. نرمالیته اسید با استفاده از رابطه زیر بهسادگی حاصل میشود.
نتایج آزمایش
- با استفاده از رابطه فوق با داشتن حجم اسید ، حجم و نرمالیته باز میتوان نرمالیته اسید را بدست آورد.
- با معلوم بودن حجم باز و نرمالیته و حجم اسید بهراحتی میتوان نرمالیته باز را محاسبه کرد.
- در رابطه فوق برای حجم از هر واحدی میتوان استفاده کرد، مشروط بر اینکه هر دو حجم ( یعنی اسید V و باز V) دارای یک واحد باشند.
- در محلول که دارای نرمالیته یکسان باشند، با حجمهای مساوی بر یکدیگر اثر میکنند.
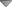
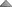
کروماتوگرافی لایه نازک(Thin Layer Chromatography) (TLC)
کروماتوگرافی لایه نازک نوعی کروماتوگرافی جذبی جامد – مایع است و اصول آن مانند کروماتوگرافی ستونی است. ولی در این مورد جسم جاذب جامد را به صورت یک لایه نازک در روی یک قطعه شیشه یا پلاستیک محکم پخش میکنند. یک قطره از محلول نمونه یا مجهول را در نزدیکی لبه صفحه میگذارند و صفحه را همراه مقدار کافی از حلال استخراج کننده در ظرفی قرار میدهند. مقدار حلال باید آنقدر باشد که فقط به سطح زیر لکه برسد (شکل الف). حلال به طرف بالای صفحه میرود و اجزاء مخلوط را با سرعتهای متفاوت با خود میبرد. در نتیجه ممکن است تعدادی لکه روی صفحه ظاهر شود. این لکه ها روی یک خط عمود بر سطح حلال ظرف قرار میگیرند (شکل ب).

این روش کروماتوگرافی بسیار آسان است و به سرعت هم انجام میشود. این روش برای تفکیک اجزاء یک مخلوط بسیار مفید است و همچنین میتوان از آن برای تعیین بهترین حلال استخراج کننده جهت کروماتوگرافی ستونی استفاده کرد.
در TLC میتوان از همان مواد جامد که در کروماتوگرافی ستونی استفاده میشود استفاده کرد و در این میان سیلیکا و آلومینا بیشتر به کار میرود. معمولا جسم جاذب را با مقدار کمی از ماده نگهدارنده مانند گچ شکسته بندی، کلسیم سولفات و یا نشاسته مخلوط میکنند تا جسم جاذب چسبندگی لازم را پیدا کند و به صفحه بچسبد. صفحه ها را میتوان قبل از مصرف تهیه کرد و یا از ورقه های پلاستیکی آماده که در بازار موجود است استفاده نمود.
یکی از مزایای مشخص TLC آن است که احتیاج به مقدار بسیار کمی از نمونه دارد. در بعضی موار میتوان تا مقدار 9-10 گرم را تشخیص داد. اما ممکن است اندازه نمونه تا 500 میکرو گرم برسد. در نمونه های زیاد میتوان از تجربه های تهیه ای استفاده کرد. در این تجربه ها لکه های مختلف را میتراشند و با یک حلال مناسب میشویند (استخراج میکنند). و برای شناسایی (از طریق طیف سنجی) به کار میبرند.
تشخیص لکه های رنگین در روی کروماتوگرام آسان است و برای تعیین محل لکه های اجسام بیرنگ روشهای متعددی وجود دارد. برای مثال میتوان با تابش نور ماوراء بنفش به صفحه محل لکه، ترکیبهایی را که خاصیت فلوئورسانس دارند مشخص کرد. به روش دیگر میتوان جسم جاذب را با ماده فلوئورسانس دار بی اثر دیگری مخلوط کرد. هنگامی که نور ماوراء بنفش به این صفحه بتابد، لکه اجسامی که نور ماورای بنفش را جذب میکنند ولی خاصیت فلوئورسانس ندارند در زمینه فلورسانس دار صفحه به صورت تیره رنگ ظاهر میشوند. در بسیاری موارد دیگر، از معرفهای آشکارساز دیگری استفاده میکنند. این معرفها را میتوان بر روی کروماتوگرام پاشید و لکه ها را ظاهر کرد. سولفوریک اسید، که بسیاری از ترکیبات آلی را به ذغال تبدیل میکند و محلول پتاسیم پرمنگنات نمونه هایی از معرفهای آشکار ساز هستند که به این روش مصرف میشوند. ید نیز معرف آشکار ساز دیگری است که مصرف میشود. در این مورد صفحه را در ظرفی میگذارند که محیط آن از بخار ید اشباع باشد. بسیاری از ترکیبات آلی ید را جذب میکنند و لکه آنها روی کروماتوگرام رنگین (معمولا قهوه ای) میشود.
در شرایط معین سرعت حرکت ترکیب نسبت به سرعت پیشرفت حلال (Rf) خاصیت مشخصی از ترکیب است. برای تعیین این مقدار مسافتی را که جسم از خط شروع تا وسط لکه را طی کرده است اندازه میگیرند و آنرا به مسافتی که حلال پیموده تقسیم میکنند. این مسافت را با خط شروع یکسانی میسنجند.

بخش عملی
تفکیک مواد رنگی برگ سبز
چند میلی لیتر از مخلوط 2 به یک اتر نفت و اتانول را همراه با چند برگ سبز در هاونی بگذارید و برگها را با دسته هاون له کنید. مایع بدست آمده را به یک قیف جدا کننده منتقل کنید و همان حجم آب مقطر به آن اضافه کنید و تکان دهید. فاز آبی پایینی را دور بریزید. این شستشو را دو بار انجام دهید و هر بار فاز آبی را دور بریزید. و آب تازه اضافه کنید.لایه آلی (بالایی) را به ارلن کوچکی منتقل کنید و به آن 2 گرم سدیم سولفات بدون آب اضافه کنید (برای آب گیری).
یک نوار 10 سانتی از ورقه کروماتوگرام سیلیکاژل تهیه کنید و یک لکه 1 الی 2 میلی متری از محلول ماده رنگی را طوری بر روی صفحه قرار دهید که حدود 1 و نیم سانتی متر از انتهای آن فاصله داشته باشد (برای گذاشتن لکه از لوله مویین تمیز استفاده کنید). صبر کنید تا لکه خشک شود. برای جداسازی، از حلال بنزن – استون با نسبت 7 – 3 (حجمی) مطابق توضیحات بالا استفاده کنید.
ممکن است تا هشت لکه رنگین مشاهده شود. این لکه ها به ترتیب کاهش مقدار Rf عبارتند از کاروتنها (دو لکه نارنجی)، کلروفیل a (آبی – سبز)، کلروفیل b (سبز) و زانتوفیلها (چهار لکه زرد).
کروماتوگرافی ستونی (Column Chromatography)
در کروماتوگرافی ستونی جسم بین فازهاى مایع و جامد پخش میشود. فاز ساکن جسم جامدی است و این جسم اجزای مایعی را که از آن میگذرد به طور انتخابی در سطح خود جذب میکند و آنها را جدا میکند. اثرهایی که باعث جذب سطحی میشوند همان اثرهایی هستند که موجب جذب در مولکولها میشوند. این اثرها عبارتند از: جاذبه الکترواستاتیکی، ایجاد کمپلکس، پیوند هیدروژنی، نیروی واندروالس و غیره.
برای جدا کردن یک مخلوط با کروماتوگرافی ستونی، ستون را با جسم جامد فعالی (فاز ساکن) مانند آلومینا یا سیلیکاژل پر میکنند و کمی از نمونه مایع را روی آن میگذارند. نمونه ابتدا در بالای ستون جذب میشود. سپس حلال استخراج کننده ای را در داخل ستون جریان میدهند. این فاز مایع متحرک، اجزای مخلوط را با خود میبرد. ولی به علت نیروی جاذبه انتخابی فاز جامد، اجزای مربوط میتوانند با سرعتهای مختلفی به طرف پایین ستون حرکت کنند. ترکیبی که با نیروی کمتری جذب فاز ساکن شود سریعتر خارج میشود زیرا که درصد مولکولی آن در فاز متحرک از ترکیبی که با نیروی زیادتری جذب فاز ساکن میشود بیشتر است.

اجزای تفکیک شده را میتوان مجددا به دو روش به دست آورد:
1) مواد جامد ستون را میتوان خارج کرد و قسمتی از آنرا که حاوی باند مورد نظر است برید و با حلال مناسب استخراج کرد.
2) چون باندها با زمانهای مختلفی خارج میشوند میتوان آنقدر حلال را از ستون عبور داد تا باندها از انتهای آن خارج شوند و در ظرف جداگانه ای بریزند.
معمولا روش دوم کاربرد بیشتری دارد.
در مورد اجسام رنگین میتوان باندهایی را که به طرف پایین ستون می آیند مستقیما مشاهده کرد.

اما در مورد اجسام بیرنگ نمیتوان تغییرات را مستقیما مشاهده کرد. با این حال بسیاری از اجسام در هنگام تابش نور ماورای بنفش فلوئورسانس پیدا میکنند و در چنین مواردی از این خاصیت جهت مشاهده باندها استفاده میشود. معمولا برای پی بردن به جریان عمل کروماتوگرافی ستونی حجمهای کوچک و ثابتی (مثلا 25 میلی لیتر) از محلول استخراج شده را جمع آوری میکنند. سپس حلال آنها را تبخیر میکنند تا ببینند جسمی در آنها وجود دارد یا خیر. گرچه ممکن است یک جسم در چند ظرف پخش شود، ولی اگر حجم هر جزء نسبتا کم گرفته شود (مثلا کمتر از 10% حجم ستون) معمولا باندهای مختلف در ظروف مختلف جمع آوری میشوند. روش دیگری که برای پی بردن به وضع تفکیک مناسب آن است که محلول استخراج شده در فاصله زمانی مختلف با کروماتوگرافی لایه نازک مورد بررسی قرار گیرد.
تعدادی از جاذبهای جامدی که عموما مصرف میشوند عبارتند از: آلومینا، سیلیکاژل، فلورسین، زغال چوب، منیزیم اکسید، کلسیم کربنات، نشاسته و شکر. معمولا شیمیدانهای آلی از آلومینا، سیلیکاژل و فلورسین بیشتر استفاده میکنند.
آلومینا (Al2O3) ترکیب قطبی بسیار فعالی است که قدرت جذب زیادی دارد و به سه صورت موجود است: خنثی، شسته شده با اسید و شسته شده با باز. آلومینای بازی برای ترکیبهای اسیدی و آلومینای اسیدی برای ترکیبهای بازی قدرت تفکیک خوبی نشان میدهد. در ترکیبهایی که به شرایط اسیدی و بازی حساسیت دارند و واکنش شیمیایی دارند باید از آلومینای خنثی استفاده کرد. آلومینا با قطبیت زیادی که دارد ترکیبهای قطبی را به شدت جذب میکند و در نتیجه ممکن است استخراج آنها از ستون را مشکل کند. فعالیت (قدرت جذب) آلومینا را میتوان با افزایش کمی آب کاهش داد، درجه فعالیت آلومینا با درصد وزنی آب موجود مشخص میشود. سیلیکاژل و فلورسین هم قطبی هستند ولی قطبیت آنها از آلومینا کمتر است.
برای اینکه جاذبهای جامد نیروی موثرتری داشته باشند، باید اندازه ذرات آنها یکنواخت و سطح مخصوص آنها زیاد باشد. چنین سطحی باعث تسریع تعادل جسم در دو فاز میشود. این حالت در ایجاد باندهای باریک اهمیت دارد.
در تعیین شرایط یک تجربه کروماتوگرافی باید به ماهیت فاز مایع (حلال) مصرفی توجه کرد. حلال نیز میتواند در جسم جامد جذب شود و به این وسیله برای جذب مواضع جذبی که در سطح جامد وجود دارند، با جسم حل شده رقابت کند. چنانچه حلال قطبی تر باشد و شدیدتر از اجزای مخلوط جذب شود، تقریبا تمام اجزاء در فاز مایع متحرک باقی میمانند و تفکیکی که در ضمن تجربه صورت میگیرد ناچیز خواهد بود. در نتیجه برای این که تفکیک خوب انجام شود باید قطبیت حلال استخراجی به طور قابل ملاحظه ای کمتر از اجزای مخلوط باشد. به علاوه باید اجزای مخلوط در حلال حل شوند، زیرا در غیر این صورت اجزا به طور دایم در فاز ساکن ستون جذب میشوند و در آن باقی میمانند. قدرت استخراجی حلالهای مختلف (یعنی توانایی آنها در انتقال یک جسم معین به پایین ستون) بترتیب زیر از بالا به پایین زیاد میشود:
در یک کروماتوگرافی ستونی ساده نمونه را در بالای ستون میگذارند و در طول تفکیک از حلال واحدی استفاده میکنند. بهترین حلال انتخابی، حلالی است که بیشترین فاصله را در باندها ایجاد کند. چون احتمالا بهترین حلال در اثر تجربه بدست می آید، گاهی راحتتر است که در انتخاب حلال برای کروماتوگرافی ستونی از روش کروماتوگرافی لایه نازک استفاده شود. تعداد زیادی از تجربه های کروماتوگرافی لایه نازک را میتوان با استفاده از حلالهای مختلف، در زمان نسبتا کوتاهی انجام داد. معمولا بهترین حلال یا مخلوط حلالی که به این روش به دست می آید برای کروماتوگرافی ستونی مناسب است.
معمولا از روشی که به استخراج تدریجی (یا جزء به جزء) معروف است استفاده میشود. در این روش برای ظهور کروماتوگرام از یک سری حلالهایی استفاده میکنند که قطبیت آنها مرتبا رو به افزایش میرود. در شروع با یک حلال غیر قطبی (معمولا هگزان) ممکن است یک باند به طرف پایین ستون حرکت کند و از آن خارج شود و در این حال باندهای دیگر در نزدیکی ابتدای ستون باقی بمانند. سپس حلالی که قطبیت آن اندکی بیشتر است به کار میبرند. در حالت ایده آل باید یک باند دیگر خارج شود و در این حال بقیه باندها در عقب آن باقی بمانند. چنانچه قطبیت حلال یکباره زیاد بالا رود، ممکن است تمام باندهایی که باقی مانده اند یکباره از ستون خارج شوند. بنابر این باید در هر مرحله قطبیت حلال به مقدار کم و با قاعده معینی افزایش یابد. بهترین راه انجام این کار آن است که از حلالهای مخلوط استفاده شود و تعویض کامل حلال چندان مناسب نسیت.
طریقه پر کردن ستون بسیار اهمیت دارد زیرا ستونی که خوب پر نشود اجزاء را هم خوب تفکیک نمیکند. جسم پرشده باید همگن باشد و در آن هوای محبوس یا حباب بخار وجود نداشته باشد.
آماده سازی ستون کروماتوگرافی
یک بورت 50 میلی لیتری را در حالت عمودی به گیره ای ببندید. شیر بورت باید بسته و چرب نشده باشد. بورت را با اتر نفت (60-30 درجه ) تا نزدیکی درجه 40 میلی لیتری آن پر کنید و به کمک یک لوله شیشه ای طویل کمی پشم شیشه را به انتهای بورت فرو برید. درون بروت به حدی شن بریزید تا ارتفاع 1 سانتی متری بالای پشم شیشه را بپوشاند. پس از خروج کامل حبابهای درون شن، در حالی که به آرامی به دیواره بورت ضربه میزنید 15 گرم آلومینا را به داخل لوله بریزید. هنگام پایین رفتن آلومینا ستون را تکان دهید. این اعمال به پر شدن یکنواخت ستون کمک میکنند. جدار داخلی بورت را که آلومینا به آن چسبیده با اتر نفت اضافی بشویید. برای محافظت از آلومینای پر شده یک لایه 1 سانتی متری شن در بالای ستون قرار دهید. شیر بورت را باز کنید و بگذارید تا حلال خارج شود و درست به بالای لایه شن بالایی برسد. حال ستون برای قرار دادن نمونه مخلوط مورد تفکیک آماده است.
کروماتوگرافی (Chromatography)
کروماتوگرافی بر اصول کل پخش فاز بنیان نهاده شده است. به طور خلاصه، در این روش جریان یک فاز از کنار (یا از داخل) فاز ساکنی میگذرد و در این حال فاز ساکن اجزای آنرا به طور انتخابی خارج میکند. این خروج یک عمل تعادلی است و مولکولهای اجزاء دوباره داخل فاز متحرک میشوند. هنگامی که ثابت پخش دو یا چند جزء در این دو فاز با هم متفاوت باشند، اجزای مربوط در فاز متحرک از هم تفکیک میشوند. به طور ساده میتوان گفت که هر چه فاز ساکن یک جزء را محکمتر نگه دارد، در صد مولکولهای جزئی که بی حرکت نگه داشته شده بیشتر میشود. جزء دیگری که با شدت کمتر نگه داشته میشود نسبت به جزء اول در فاز متحرک درصد مولکولی بیشتری خواهد داشت. بنابراین به طور متوسط مولکولهای جزئی که با شدت کمتر نگه داشته میشوند، نسبت به مولکولهای دیگر با سرعت بیشتری از روی فاز ساکن میگذرند (در جهت جریان) و در نتیجه اجزای مربوط به قسمتهای مختلف فاز ساکن (باندها) منتقل میشوند.
فاصله باندها به طور خطی به مسافتی که در ستون طی میشود بستگی دارد. به طور کلی هر چه مسافت طی شده بیشتر باشد، فاصله باندها زیادتر خواهد شد. یادآور میشود که اجزای مخلوط باید ضرایب پخش متفاوتی داشته باشند تا بتوان آنها را به کمک پخش فاز تفکیک کرد. در صورتی که این ضرایب به هم نزدیک باشند، اجزای مربوط فقط به طور جزئی به باندهای جداگانه تفکیک میشوند. البته میتوان طول مسیر را زیاد کرد و به اجزاء فرصت داد تا بیشتر از هم جدا شوند.
کروماتوگرافی چهار نوع مهم دارد که بر اصول توصیف شده بالا متکی هستند. این انواع عبارتند از:
کروماتوگرافی گازی (کروماتوگرافی تفکیکی گاز مایع) (Gas Chromatography)
کروماتوگرافی ستونی (Column Chromatography)
کروماتوگرافی لایه نازک (Thin Layer Chromatography) (TLC)
کروماتوگرافی کاغذی(Paper Chromatography).
شعله ور کردن شکر بدون آتش
در نیمه زیرین یک ظرف، بلور پتاسیم کلرات و در نیمه بالایی شکر قرار میدهیم
حالا میتوانیم از بقیه بخواهیم از شکر بچشند وببینند که واقعا شکر است
حال یک همزن یا یک عصای شعبده بازی که قبلا به اسید سولفوریک آغشته شده را به ظرف حاوی شکر(در واقع پتاسیم کلرات) نزدیک میکنیم واینطوری شما میتوانید شکر را بدون آتش شعله ور کنید
نکته: این آزمایش را هیچ وقت در یک فضای بسته انجام ندهید برای انجام آن حتما از فضای باز استفاده کنید.

با سلام . به وبگاه رسمی علم و دانش خوش آمدید ! من شایان شیت ره هستم دانش آموز دبیرستان سلام صادقیه ! این پروژه تحقیقی بنده است . تا این جا 77 مطلب ثبت گردیده . امید وارم از این مطالب نهایت استفاده رو ببرید . با تشکر مدیریت !
بازدید دیروز : 13
کل بازدید : 46119
کل یاداشته ها : 77